通化東寶:痛風一類新藥THDBH151片申報臨床獲得受理
通化東寶藥業股份有限公司(以下簡稱“公司”、“通化東寶”)全資子公司東寶紫星(杭州)生物醫藥有限公司(以下簡稱“東寶紫星”)于近日取得國家藥品監督管理局藥品審評中心(CDE)簽發的關于THDBH151片臨床試驗申請受理通知書,受理號為CXHL2200713國、CXHL2200714國、CXHL2200715國。
THDBH151片是一款XO/Urat1雙靶點抑制劑用于治療痛風的藥物,同時也是通化東寶在研兩款治療痛風和高尿酸血癥的一類創新藥之一,另一款URAT1抑制劑(THDBH130片)已于去年成功進入臨床試驗階段。THDBH151片申報臨床獲得受理彰顯出公司在向創新藥企轉型道路上闊步前行的決心和能力。
中國高尿酸血癥和痛風患者對高效安全的抗痛風藥物仍有迫切的需求,根據《中國高尿酸血癥與痛風診療指南(2019)》,市場上現有的治療痛風藥物主要包括抑制尿酸生成的以XO為主要靶點的黃嘌呤氧化酶抑制劑(別嘌醇、非布司他)和抑制尿酸重吸收的Urat1抑制劑(苯溴馬隆、雷西那德)。這兩類藥物在有效性和安全性上都有可以改進的空間。以雷西那德為代表的新型Urat1抑制劑是近年來高尿酸血癥領域的研究熱點,但是臨床研究中發現Urat1抑制劑存在急性腎毒性問題。因此Urat1抑制劑需要與XO抑制劑聯用,從源頭上減少尿酸的生產,以減少急性腎毒性的發生。
公司THDBH151片因其在機制上的特殊優勢,既能抑制黃嘌呤氧化酶(XO),從源頭上減少尿酸產生,也可抑制腎小管URAT1轉運體對尿酸重吸收,加快尿酸排出。此外,THDBH151片通過平衡好XO/Urat1在降尿酸中的作用,在提高藥效的同時降低副作用,大幅提高患者依從性,有望成為同領域中Best-in-Class藥物。目前國內外均暫無同類產品上市。
近年來,中國高尿酸血癥及痛風患者呈明顯上升和年輕化趨勢。據《中國高尿酸血癥與痛風診療指南(2019)》及國家統計局第六次人口普查數據顯示,中國高尿酸血癥的總體患病率為13.3%,患病人數約為1.77億,痛風總體發病率為1.1%,患病人數約為1,466萬。高尿酸血癥已成為繼糖尿病、高血壓、高血脂癥后的“第四高”,痛風也已成為僅次于糖尿病的第二大代謝類疾病。
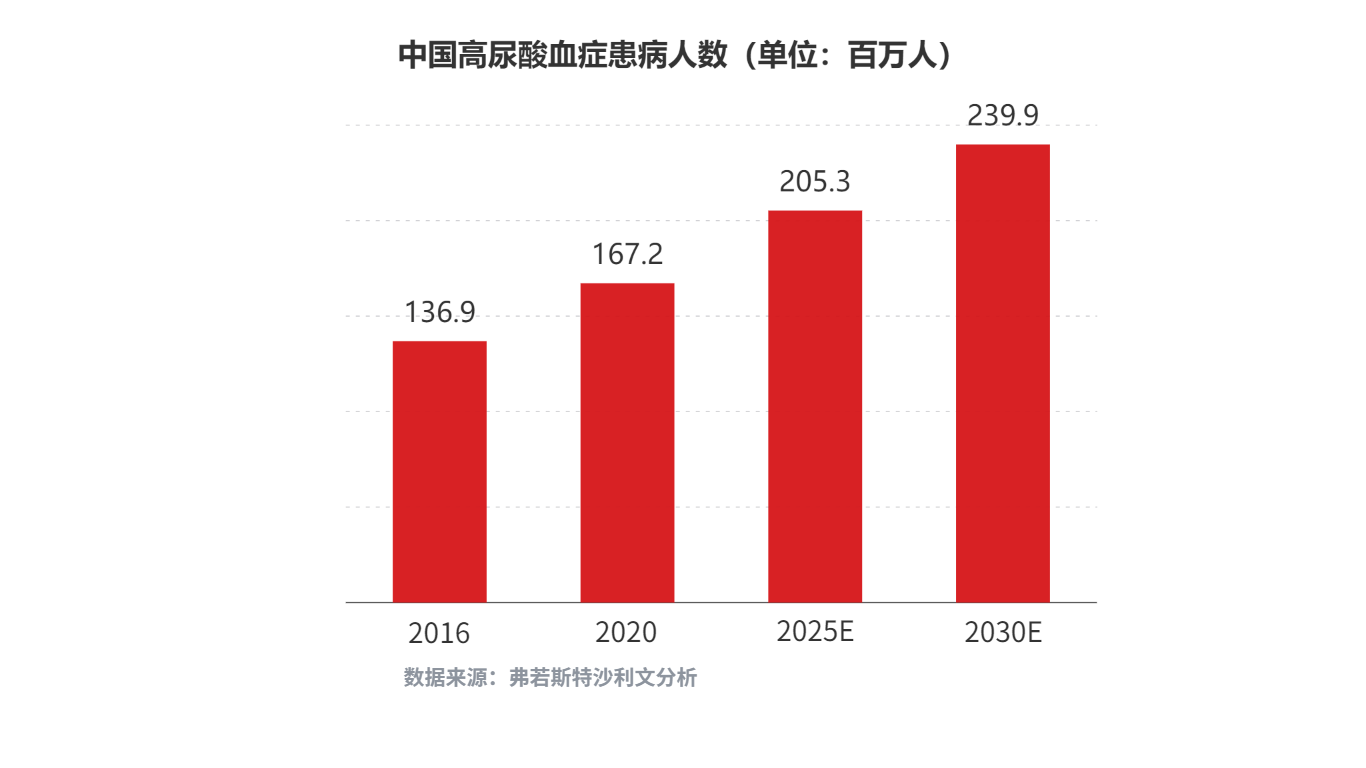
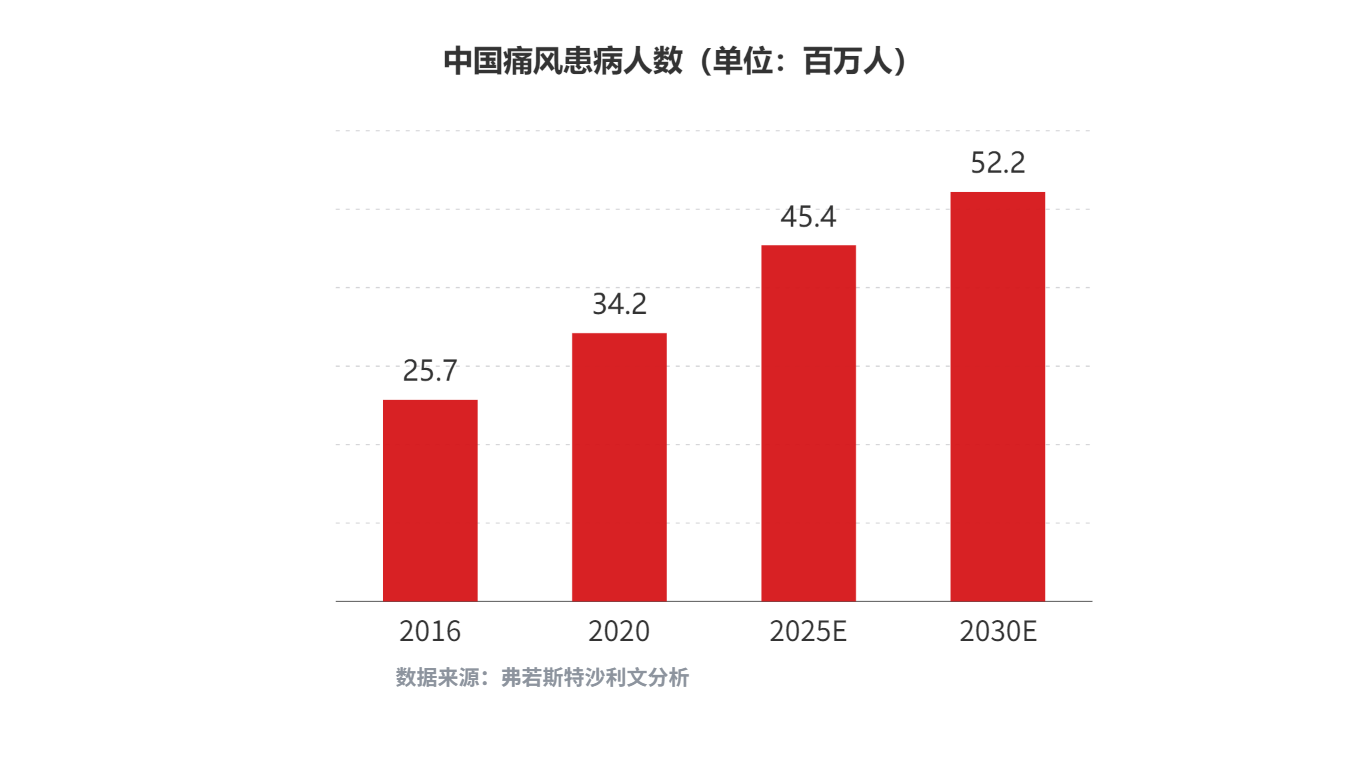
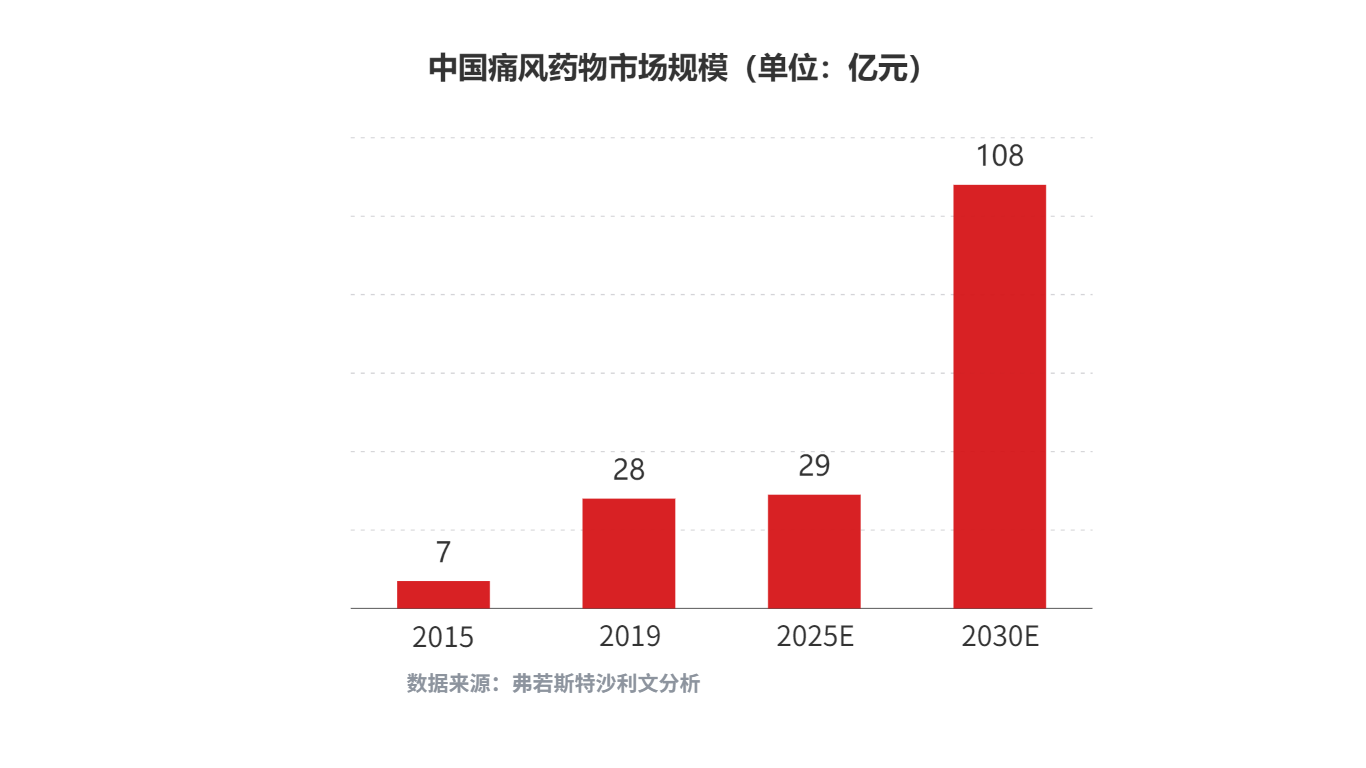
中國痛風和高尿酸血癥治療藥物市場空間廣闊。根據弗若斯特沙利文分析,未來中國高尿酸血癥和痛風患病人數會持續增加,高尿酸血癥患病人數預計在2025年/2030年將分別達到2.05億人/2.39億人;痛風患病人數預計在2025年/2030年將分別達到4,540萬人/5,220萬人;對應的中國痛風藥物市場規模預計在2025年/2030年將分別增長至29億元/108億元。
公司THDBH151片申報臨床獲得受理體現出公司在糖尿病領域外其他內分泌代謝領域的積極進展。未來公司將繼續加速推進在痛風和高尿酸血癥治療領域的研發進程,通過自主研發療效顯著且安全性高的創新藥物來開拓公司的發展邊界,打造新的增長引擎,并與公司現有業務形成協同效應,構筑新的發展空間。









